ПРОИЗВОДИТЕЛИ 3D-ПЕЧАТНЫХ ИМПЛАНТАТОВ, ПОСТАВЩИКИ И ПРОДАВЦЫ АДДИТИВНЫХ СИСТЕМ ДОЛЖНЫ ОБЕСПЕЧИТЬ БЕЗОПАСНОСТЬ И ВОСПРОИЗВОДИМОСТЬ СВОЕЙ ПРОДУКЦИИ. ВАЛИДАЦИЯ ПРОЦЕССОВ АДДИТИВНОГО ПРОИЗВОДСТВА ЯВЛЯЕТСЯ ТЕМОЙ НОВОГО ТЕХНИЧЕСКОГО ДОКУМЕНТА, ОПУБЛИКОВАННОГО TÜV SÜD.
Сертификационная компания TÜV SÜD выпустила первое в отрасли руководство по 3D-печати для многократного производства медицинских изделий, безопасных и пригодных для использования по назначению.
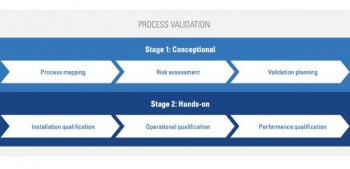
Опубликованное в виде "белой книги", руководство описывает стандарты, которые производители должны соблюдать на каждом этапе рабочего процесса, а также полномочия, необходимые для их применения на практике. По словам TÜV SÜD, путем сжатия соответствующих нормативных актов в упрощенном формате она стремится "описать возможные процедуры" и "указать на существующие пробелы" для тех, кто работает как в области 3D-печати, так и в клинических условиях.
Хотя стандарты ISO 9001 и 13485 часто используются в медицинском производстве и представляют собой надежные системы управления качеством (QMS), они не способны решить уникальные проблемы 3D-печати в конкретном секторе. Именно поэтому TÜV SÜD опубликовала собственную технологическую цепочку, от квалификации до последующей обработки, которая подчеркивает шаги, которые необходимо предпринять производителям для обеспечения соответствия требованиям при 3D-печати медицинских деталей.




