Об использовании 3D-печати в медицине известно уже давно: еще в конце 1990-х годов компания Align Techno-logy начала производить капы для выравнивания зубов с использованием 3D-принтеров. Однако первый имплантат удалось напечатать лишь в 2012 году бельгийской фирме LayerWise. Тогда же состоялась первая операция по вживлению титановой нижней челюсти, изготовленной с помощью 3D-печати.
Для российской медицины 3D-печать все еще остается достаточно экзотической технологией, однако интерес к ней растет с каждым годом, поскольку все больше врачей видит преимущества использования аддитивных технологий в травматологии и ортопедии, в нейрохирургии, в онкологии, в челюстно-лицевой хирургии и так далее.
В настоящее время 3D-печать с успехом используется в самых сложных случаях по замещению костных дефектов, когда стандартные изделия не позволяют решить проблему.
Напечатанные имплантаты являются цельной титановой конструкцией, спроектированной индивидуально по снимкам компьютерной томографии пациента. Они обладают высокими эксплуатационными характеристиками благодаря своей целостности и имеют пористую структуру поверхности, способствующую наилучшей интеграции имплантата в костные ткани. Серийные имплантируемые изделия, изготовленные с применением печати, также обладают высокими эксплуатационными качествами и высоким уровнем остеоинтеграции благодаря наличию ячеистой структуры поверхности. Кроме того — об этом свидетельствует, в частности, опыт российской команды инженеров CML AT Medical и медиков — стоимость их производства приближается к стоимости серийного производства традиционными технологиями и продолжает снижаться благодаря удешевлению материалов и повышению производительности 3D-принтеров.
Помимо имплантатов 3D-печать позволяет производить анатомические модели костей, органов и сосудов, которые используются в планировании операций и в обучении. В том числе благодаря аддитивным технологиям стало возможным печатать хирургические шаблоны и направляющие, которые проектируются индивидуально под пациента, персонифицируют процесс проведения операции, снижая ее травматичность, повышая точность и ускоряя процесс реабилитации. Например, инженерами нашей компании проектируются анатомические модели «сложных» опухолей. Эти модели используются в том случае, когда результатов 3D-визуализации компьютерной томографии недостаточно для определения стратегии хирургического вмешательства. Нельзя также обойти стороной такое применение 3D-печати, как печать прототипов медицинских инструментов и устройств — благодаря своим широким возможностям и потенциалу аддитивные технологии позволяют значительно ускорить выведение нового медицинского продукта на рынок.
Из всего пула доступных технологий 3D-печати и материалов активно используются лишь некоторые виды. Это обусловлено требованиями к безопасности и биосовместимости материалов. Из пластиковых материалов инженеры и медики чаще всего отдают предпочтение прозрачным прочным полимерам, эластичным полимерам, полиамиду, полипропилену, ABS, PLA, технологии SLA, SLS, FDM; из металлов — титану, кобальт-хрому, медицинской стали и технологии SLM и EBM. Причем EBM наилучшим образом подходит для производства серийных изделий в силу специфики технологии печати, при которой можно заполнять камеру изделиями целиком, а SLM — для индивидуальных.
Процесс производства индивидуального имплантируемого изделия является многостадийным. Его можно условно разделить на 3 крупных блока: проектирование, 3D-печать, постобработка.
Проектирование начинается с получения инженерами КТ снимков анатомической области (рис. 1). После сегментирования снимков в специализированном программном обеспечении инженер получает 3D-геометрию костного дефекта.
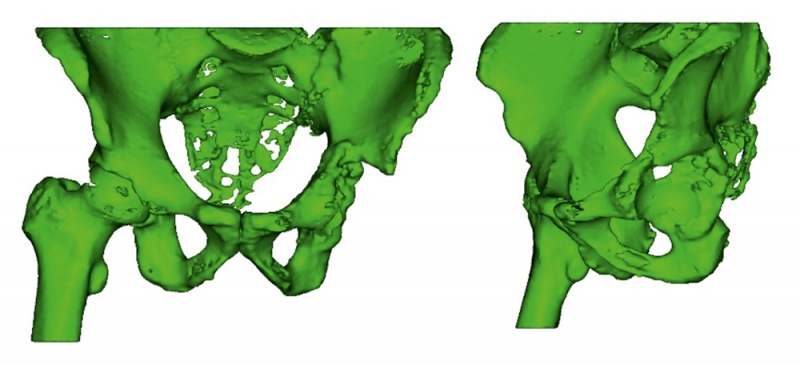 Рис. 1. Результат сегментации КТ снимков таза
Рис. 1. Результат сегментации КТ снимков таза
На следующем этапе происходит определение требований и ограничений для проектируемого изделия с врачом (рис. 2): описание техники операции, место установки и крепления, тип крепления, сопутствующие медицинские изделия, с которыми требуется обеспечить совместимость имплантата (например, вкладыши, импакторы), пожелания по облегчению конструкции, поверхности с ячеистой структурой. После уточнения этих требований инженер может приступить к проектированию. Для каждого вида изделий существуют свои этапы промежуточного контроля, на которых изделие отправляется на согласование врачу.
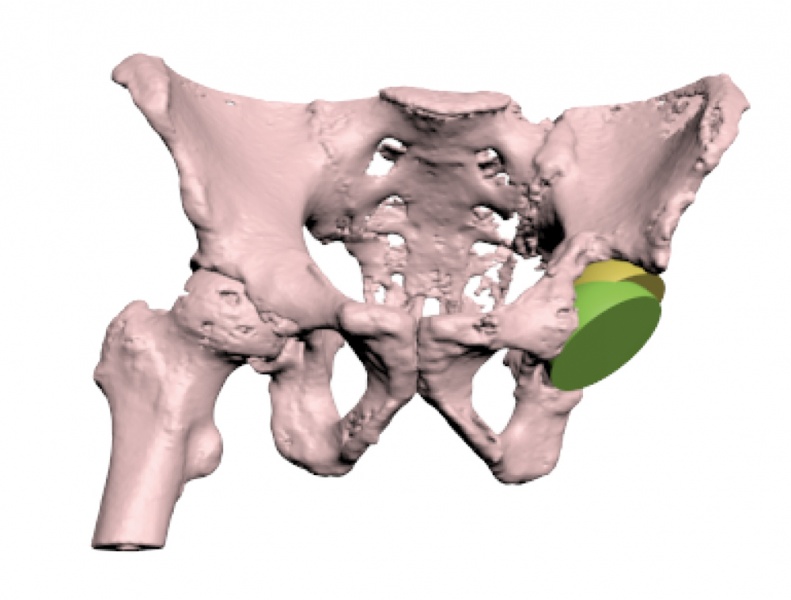

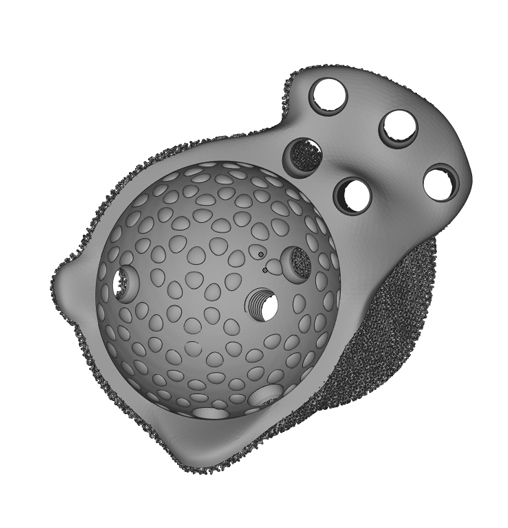
Рис. 2. Процесс проектирования на примере тазобедренной чашки
В данном итерационном процессе врач уточняет требования, в геометрию изделия вносятся необходимые корректировки. После согласования финальной геометрии проводится виртуальная проверка функциональности, технологическая проработка и разработка вспомогательных графических материалов для проведения операции, а после файл с финальной 3D-геометрией изделия направляется на печать.
В CML AT Medical при проектировании медицинских изделий мы четко разграничиваем зоны ответственности между врачом и инженером. С одной стороны, врач определяет и согласовывает требования к изделию, исходя из техники проведения операции и состояния окружающих тканей. С другой — существует множество технических особенностей проектирования, которые учитывает инженер: зарастание отверстий, удаляемость порошка, технологические припуски на механическую обработку, тонкие стенки. При таком разделении труда в процессе проектирования будущий результат будет обладать требуемым качеством.
После утверждения 3D-геометрии изделия врачом модель отправляется на печать (рис. 3). Ее запуску предшествует подготовительный этап, на котором инженер производства проверяет модель на наличие ошибок и на производимость. Затем проектируется расположение изделия на платформе 3D-принтера с учетом технологических ограничений, строятся поддержки. На данном этапе одна из важнейших задач инженера — построить поддержки в необходимом и достаточном количестве, чтобы, во‑первых, обеспечить максимальное отведение тепла и закрепление изделия на платформе, а во‑вторых, не увеличить стоимость изделия, сэкономить материал и не усложнить дальнейшую механическую обработку.
 Рис. 3. Тазобедренная чашка, изготовленная по технологии SLM из Ti6Al4V
Рис. 3. Тазобедренная чашка, изготовленная по технологии SLM из Ti6Al4V
Процесс 3D-печати может занять от нескольких часов до нескольких дней в зависимости от объема изделий, размещенных на платформе. Если речь идет о технологии SLM, то для снятия термических напряжений после печати платформу с изделиями дополнительно на сутки помещают в вакуумную печь. После термической обработки начинается финальный этап — механическая обработка изделия. Итогом становится готовое изделие, которое после отмывки и стерилизации направляется врачу для имплантирования пациенту. На данном этапе изделие отделяют от платформы, удаляют поддержки, проводят необходимую механическую обработку отверстий, если это предусмотрено требованиями к изделию (нарезка резьбы, обработка/расточка отверстий, полировка, маркировка и прочее).
Имплантируемые медицинские изделия относятся к самому высокому классу опасности, необходимо обеспечить их максимальную безопасность для пациента: они должны быть прочными и биосовместимыми. Чтобы обеспечить биосовместимость, крайне важно, чтобы в 3D-принтере на всем жизненном цикле использовался порошок только одного сплава. При использовании порошков разных сплавов на одном 3D-принтере невозможно обеспечить 100% удаляемость этого порошка из камеры, существует риск попадания микрочастиц порошка сплава, который не является биосовместимым, в будущее медицинское изделие. При установке такой имплант может вызвать негативную реакцию организма, что приведет к удалению имплантата и повторной операции. Подобные требования по чистоте также применяются к этапам пескоструйной и механической обработки.
Процесс очистки любых медицинских изделий является многостадийным, он включает в себя многостадийную мойку и ультразвуковую мойку в спиртосодержащем агенте.
В итоге процесс производства индивидуального медицинского изделия от момента получения КТ снимков пациента до отгрузки готового изделия занимает в среднем 2 недели.
Аддитивные технологии в медицине — рынок сравнительно новый не только для России, но и для всего мира. Сейчас активно меняется законодательство в США, Китае, Европе, разрабатываются рекомендации по применению 3D-печати, выдаются разрешения на внедрение, лицензируются компании. Важно, чтобы и Россия не отстала от данного мирового тренда, чтобы на отечественном рынке был принят свой стандарт по применению напечатанных медицинских изделий. Тем более что успешные компании и стартапы, занимающиеся аддитивными технологиями, уже существуют. Так, к примеру, стартап CML AT Medical успешно работает сразу в шести направлениях: от изготовления индивидуальных эндопротезов с добавлением ячеистых структур для лучшей остеоинтеграции до позвоночных кейджей, челюстных и краниопластин. Дальнейшее совершенствование российского законодательства в этой сфере сняло бы множество административных барьеров по закупке медицинскими учреждениями таких конструкций, значительно расширило бы рынок и повысило качество и технологичность медицинской помощи. ■
 Автор: Яна Чекрыжова, генеральный директор ООО «ЛВМ АТ Медицина»
Автор: Яна Чекрыжова, генеральный директор ООО «ЛВМ АТ Медицина»
Источник журнал "Аддитивные технологии" № 3-2020



